PEMBUATAN TABLET EKSTRAK JAHE MERAH (ZINGIBER OFICINALE ROXB)
- Dapatkan link
- X
- Aplikasi Lainnya
BAB I
PENDAHULUAN
A.
Latar Belakang
Tumbuhan telah memberikan banyak manfaat bagi kehidupan
manusia, baik untuk keperluan sehari-hari maupun sebagai obat. Memasuki abad
ke-20, kira-kira 100 tahun yang lalu, pabrik farmasi terlibat aktif dalam
pengembangan ekstraksi, penelitiandan pemasaran senyawa aktif yang berasal dari
tumbuhan obat (Supriyanti, dkk., 2014).
Salah satu tumbuhan tradisional yang digunakan untuk obat
diantaranya adalah tumbuhan jahe merah. Jahe merah (Zingiber officinale Roxb)
merupakan salah satu dari temu-temuan suku Zingiberaceae yang berperan penting
dalam berbagai aspek di masyarakat Indonesia. Jahe merah sudah digunakan
sebagai obat secara turun-temurun karena mempunyai komponen volatil (minyakatsiri)
dan non volatil (oleoresin) paling tinggi jika dibandingkan dengan jenis jahe
yang lain yaitu kandungan minyak atsiri sekitar 2,58-3,90% dan oleoresin 3%. Jahe
digunakan untuk berbagai penyakit, termasuk mabuk perjalanan, gangguan
pernapasan dan gastrointestinal (Zamroni Salim, Ph.D dan
Ernawati Munadi, Ph.D : 2017).
Survei yang dilakukan di apotek, sediaan simplisia dan
ekstrak herbal jahe merah ada beberapa yang sudah dalam bentuk sediaan padat
antara lain jahe merah dalam bentuk sediaan kapsul, sirupdan tablet. Salah satu
contoh sediaan jahe merah antara lain Antangin JRG+Jahe Merah® (PT. Deltomed),
Obana ®(PT. Hermed), Vitamam I dan Obasa ® (PT. Hermed). Dimana setiap sediaan
herbal tersebut ada yang digunakan untuk obat batuk, obat pelangsing, meningkatkan
stamina, mual dan muntah dan lain sebangainya.
Proses pembuatan tablet bahan obat dan zat-zat tambahan
umumnya berupa serbuk yang tidak dapat langsung dicampur dan dicetak menjadi
tablet karena akan langsung hancur dan tablet mudah pecah. Campuran serbuk itu
harus diubah dalam bentuk granul, yaitu kumpulan serbuk dengan volume lebih
besar yang saling melekat satu sama lain. Bahan pengikat adalah yang bertangung jawab untuk kekompakan dan daya
tahan dari tablet. Dari itu bahan pengikat mengurus penyatuan bersama dari
partikel serbuk dalam sebuah butir granulat (Ansel : 2014).
Berdasarkan uraian
diatas peneliti tertarik untuk membuat sediaan tablet dan pengaruh bahan
pengikat pada pembuatan sediaan tablet ekstrakjahe merah yang dikombinasi dengan
vitamin B6 dengan metode granulasi basah dengan berbagai jenis bahan pengikat.
Bahan pengikat yang digunakan yaitu PVP, amilum manihot dan gelatin. Penambahan
vitamin B6 dikarenakan menurut sebuah penelitian pengobatan menggunakan serbuk
jahe merah 500 mg dengan vitamin B6 10 mg efektif mengurangi mual dan muntah
(Sripamote dalam lete dan allue, 2016).
B.
Rumusan Masalah
1.
Apakah ekstrak jahe merah
(Zingiberofficinale Roxb) yang dikombinasi vitamin B6 dengan berbagai jenis dan
konsentrasi bahan pengikat dapat dibuat menjadi tablet dengan metode granulasi
basah.
2.
Apakah dapat diketahui tablet
ekstrak jahe merah yang dicetak memenuhi persyaratan evaluasi tablet.
BAB II
TINJAUAN PUSTAKA
A.
Tumbuhan Jahe Merah dan Vitamin B6
1.
Jahe merah
Jahe merupakan tanaman rempah yang dimanfaatkan sebagai
minuman atau campuran bahan pada bahan pangan. Rasa jahe yang pedas bila dibuat
minuman memberikan sensasi sebagai pelega dan penyegar tenggorokan. Tanaman
jahe termasuk kedalam kelas monocotyledone ( tanaman berkeping satu) dan family
Zingiberaceae (suku temu-temuan). Nama zingiber merupakan nama latin yang
berasal dari bahasa sanskerta yaitu “singiberia” yang mempunyai makna berbentuk
tanduk. Hal itu karena bentuk percabangan rimpangnya yang mirip tanduk rusa.
Biasanya tanaman ini tumbuh dipekarangan rumah mapun dikebun (Saparinto, 2016).
Nama asing tanaman jahe merah adalah halia, haliya padi,
haliya udang (Malaysia); luya, allam (Filipina); adu, ale, ada (India);
sanyabil (Arab); chiang, p’I, khan ciang, kiang, sheng chiang (Cina); gember
(Belanda); ginger (Inggris); gingembre, herbe au giingimbre (Perancis) .
Gambar Tumbuhan Jahe Merah
Gambar Rimpang Jahe Merah
2.
Morfologi Tumbuhan
Jahe merah merupakan terna berbatang semu tegak yang
tidak bercabang dan termasuk famili Zingiberaceae. Batang jahe merah berbentuk
bulat kecil berwarna hijau dan agak keras. Daunnya tersusun berselang-selang
teratur. Tinggi tanaman ini 30-60 cm. Jahe merah tumbuh baik didaerah tropis
yang beriklim cukup panas dan curah hujannya sedikit. Jika cahaya matahari
mencukupi, tanaman ini dapat
menghasilkan rimpang jahe lebih besar (Saparinto, 2016).
3.
Sistematika tumbuhan
Divisio :
Spermatophyta
Subdivisio :
Angiospermae
Kelas :
Monocotyledoneae
Ordo :
Zingiberales
Famili :
Zingiberaceae
Genus : Zingiber
Species :
ZingiberofficinaleRoxb
4.
Kandungan Kimia
Komponen senyawa kimia yang terkandung dalam jahe terdiri
dari minyak menguap, minyak tidak menguap, dan pati. Minyak menguap biasa
disebut minyak atsiri merupakan komponen pemberi bau yang khas, sedangkan
minyak tak menguap yang disebut oleoresin merupakan komponen pemberi rasa pedas
dan pahit. Komponen yang terdapat pada oleoresin merupakan gambaran utuh dari
kandungan jahe, yaitu minyak atsiri dan fixed oil yang terdiri dari zingerol,
shogaol dan resin (Setyawan, 2015)
5.
Manfaat Jahe
Jahe terkenal menghasilkan efek menghangatkan jika
dimakan, dan sifat dasarnya yang berbau tajam merangsang reseptor-reseptor
termogenik. Efek farmakologis paling pentingnya yaitu penggunaannya untuk
mencegah gejala- gejala gastrointestinal pada mabuk perjalanan dan mual pascaoperasi,
serta vertigo dan mual pagi hari pada
kehamilan dan terdapat bukti klinis khasiat jahe pada kondisi ini. Konsumsi
jahe juga telah dilaporkan memiliki efek bermanfaat meringankan nyeri dan
frekuensi sakit kepala migrain. Jahe terkenal menghasilkan efek menghangatkan
jika dimakan, dan sifat dasarnya yang berbau tajam merangsang reseptor-reseptor
termogenik (Saparinto, 2016).
6.
Vitamin B6
Gambar 1. Struktur Piridoksin Hidroklorida
Uraian tentang Piridoksin hidroklorida menurut Ditjen BKAK 2014:
Pemerian :
Hablur atau serbuk hablur putih atau hampir putih; stabil di udara; secara
perlahan-lahan dipengaruhi oleh cahaya matahari
Kelarutan :
Mudah larut dalam air; sukar larut dalam etanol; tidak larut dalam eter Vitamin
B6 selain untuk mencegah dan mengobati defesiensi vitamin
B6 dengan gejala berupa kelainan kulit, peradangan lendir
mulut dan lidah- kelainan susunan syaraf pusat dan gangguan eritopetik berupa
anemia hipokrom mikrosister juga diberikan bersama vitamin B lainnya.
B.
Simplisia dan Ekstraksi
1.
Simplisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai
obat yang belum mengalami pengolahan apapun juga dan kecuali dikatakan lain,
berupa bahan yang telah dikeringkan. Simplisia dibedakan simplisia nabati,
simplisia hewani, simplisia pelikan
(mineral). Simplisia nabati adalah simplisia yang berupa tumbuhan utuh, bagian
tumbuhan atau eksudat tumbuhan (BPOM RI, 2014).
2.
Ekstrak
Ekstraksi merupakan proses pemisahan bahan dari
campurannya dengan menggunakan pelarut. Ekstrak adalah sediaan yang diperoleh
dengan cara mengekstraksi tanaman obat dengan ukuran partikel tertentu dan
menggunakan medium pengekstraksi yang tertentu (Supriyanti, 2014).
Ekstraksi adalah kegiatan penarikan kandungan kimia yang
dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan
menggunakan pelarut cair yang sesuai. Senyawa aktif yang sesuai terdapat dalam
berbagai simplisia dapat digolongkan ke dalam golongan minyak atsiri, alkaloid,
flavanoid dan lain- lain. Diketahuinya senyawa aktif yang dikandung simplisia
akan mempermudah pemilihan pelarut dan cara ekstraksi yang tepat (BPOM RI,
2014).
Pembuatan sediaan ekstrak dimaksudkan agar zat berkhasiat
yang terdapat di simplisia terdapat dalam bentuk yang mempunyai kadar yang
tinggi dan hal ini memudahkan zat berkhasiat dapat diatur dosisnya. Adapun metode ekstraksi dengan
menggunakan pelarut, terdiri dari:
1)
Cara dingin
a.
Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan
menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur
kamar. Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah
dilakukan penyaringan maserat dan seterusnya.
b.
Perkolasi
Perkolasi adalah
ekstraksi dengan pelarut yang selalu baru, yang umumnya dilakukan pada
temperatur ruangan. Proses terdiri dari tahapan pengembangan bahan, tahapan
maserasi antara, tahap perkolasi sebenarnya (penetesan/ penampungan ekstrak),
terus menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali jumlah bahan.
2)
Cara Panas
a.
Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur
pada titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang
relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan
proses pada residu pertama sampai 3-5 kali sehingga proses ekstraksi sempurna.
b.
Sokletasi
Sokletasi adalah ekstraksi yang umumnya dilakukan dengan
alat khusus sehingga terjadi ekstraksi kontiniu dengan jumlah pelarut relatif
konstan dengan adanya pendingin balik.
c.
Digesti
Digesti adalah maserasi kinetik (dengan pengadukan
kontinu) pada temperatur yang lebih tinggi dari temperatur kamar, secara umum
dilakukan pada temperatur 40-500C.
d.
Infusa
Infusa adalah ekstraksi dengan pelarut air pada
temperatur penangas air (bejana infus tercelup dalam penangas air mendidih,
temperatur terukur 96-980C selama waktu tertentu (15-20 menit)
e.
Dekok
Dekok adalah infus
pada waktu yang lebih lama (30 menit ) dan temperatur sampai titik didih air (BPOM RI, 2014).
C.
Tablet
1.
Pengertian Tablet
Menurut FI edisi IV, tablet adalah sediaan padat
mengandung bahan obat dengan atau tanpa bahan pengisi. Tablet yang berbentuk
kapsul umumnya disebut kaplet. Bolus adalah tablet besar yang digunakan untuk
obat hewan besar. Bentuk tablet umumnya berbentuk cakram pipih/gepeng, bundar,
segitiga, lonjong dan sebagainya. Bentuk khusus ini dimaksudkan untuk
menghindari, mencegah atau mempersulit pemalsuan dan agar mudah dikenal orang (Kumoro, 2015).
Tablet adalah bentuk sediaan obat solid mengandung zat
aktif yang dapat diberikan secara oral dan ditelan, tablet yang dikunyah dulu
lalu ditelan, atau hanya dikulum/diisap. Selain tablet yang diberikan melalui
oral, terdapat juga tablet yang diberikan melalui rektal, vaginal,
implantasi-transdermal, tablet yang dilarutkan dulu lalu diminum (tablet
efervesen) karena popularitasnya yang besar dan penggunaannya yang sangat luas
sebagai sediaan obat, tablet terbukti menunjukkan suatu bentuk yang efisien,
sangat praktis dan ideal untuk pemberian zat aktif terapi secara oral (Allen,
2014).
Berdasarkan metode pembuatan, dapat digolongkan sebagai
tablet cetak dan tablet kempa. Tablet cetak dibuat dengan cara menekan massa
serbuk lembab dengan tekanan rendah kedalam cetakan. Tablet kempa dibuat dengan
memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan baja.
Kriteria sediaan tablet adalah stabil secara fisika dan kimia, secara ekonomi
dapat menghasilkan sediaan yang dapat menjamin agar setiap sediaan mengandung
obat dalam jumlah yang benar, penerimaan oleh pasien (ukuran, bentuk, rasa,
warna dan lain sebagainya) dan untuk mendorong pasien menggunakan obat sesuai
dengan aturan pemakaian obat.
Tablet yang dinyatakan baik harus memenuhi syarat, yaitu:
a.
Memiliki kemampuan atau daya tahan
terhadap pengaruh mekanis selama proses produksi, pengemasan dan distribusi.
b.
Bebas dari kerusakan seperti pecah
pada permukaan dari sisi-sisi tablet.
c.
Dapat menjamin kestabilan fisik
maupun kimia dari zat berkhasiat yang terkandung didalamnya.
d.
Dapat membebaskan zat berkhasiat
dengan baik sehingga memberikan pengobatan seperti yang dikehendaki.
2.
Komponen Tablet
Komponen atau formulasi tablet kempa terdiri atas zat
aktif, bahan pengisi, bahan pengikat, desintegran, dan lubrikan, dapat juga
mengandung bahan pewarna, bahan pengaroma dan bahan pemanis.
1)
Zat aktif : harus memenuhi syarat
yang ditentukan farmakope
2)
Eksipien atau bahan tambahan.
a. Bahan pengisi berfungsi untuk memperbesar volume massa
agar mudah dicetak atau dibuat. Bahan pengisi ditambahkan jika zat aktifnya
sedikit atau sulit dikempa. Misalnya laktosa, pati dan selulosa mikrokristal.
b. Bahan pengikat berfungsi memberikan daya adhesi pada
serbuk sewaktu granulasi serta menambah daya kohesi pada bahan pengisi,
misalnya gom akasia, gelatin, sukrosa, povidon, metilselulosa, CMC, selulosa
mikrokristal.
c. Bahan penghancur/pengembang berfungsi membantu hancurnya
tablet setelah ditelan. Misalnya pati, pati dan selulosa yang dimodifikasi
secara kimia, asam alginat, selulosa mikrokristal, dan povidon sambung-silang.
d. Bahan pelicin berfungsi mengurang gesekan selama proses
pengempaan tablet dan juga berguna untuk mencegah massa tablet melekat pada
cetakan. Misalnya senyawa asam stearat dengan logam, asam stearat dan talk.
Umumnya lubrikan bersifat hidrofob, sehingga dapat menurunkan kecepatan
disintegran dan disolusi tablet. Oleh karena itu, kadar lubrikan yang berlebih
harus dihindari. PEG dan garam lauril sulfat dapat digunakan, tetapi kurang
memberikan daya lubrikasi yang optimal dan diperlukan dalam kadar yang lebih
tinggi.
e. Glidan adalah bahan yang dapat meningkatkan kemampuan
alir serbuk, umumnya digunakan dalam kempa langsung tanpa proses granulasi.
f. Bahan penyalut
3)
Ajuvan
a. Bahan pewarna dan lak berfungsi meningkatkan nilai
estetika atau untuk identitas produk. Misalnya zat pewarna dari tumbuhan.
b. Bahan pengaroma berfungsi menutupi rasa dan bau zat
berkhasiat yang tidak enak (misalnya tablet isap penisilin), biasanya
digunakan untuk table yang penggunaannya
lama di mulut. Misalnya macam-macam minyak atsiri (Kumoro, 2015).
3.
Cara pembuatan tablet
Bahan obat dan zat-zat tambahanumumnya berupa serbuk yang
tidak dapat langsung dicampur dan dicetak menjadi tablet karena akan langsung
hancur dan tablet menjadi mudah pecah. Campuran serbuk itu harus diubah menjadi
granul-granul, yaitu kumpulan serbuk dengan volume besar yang saling melekat
satu sama lain. Tujuan granulasi adalah sebagai berikut.
1)
Supaya sifat alirnya baik (free-flowing).
Granul dengan volume tertentu dapat mengalir teratur dalam jumlah yang sama
kedalam mesin pencetak tablet.
2)
Ruang udara dalam bentuk granul
jumlahnya lebih kecil dibanding dengan bentuk serbuk jika diukur dalam volume
yang sama. Makin banyak udaranya, tablet makin mudah pecah.
3)
Agar pada saat dicetak tidak mudah
melekat pada stempel (punch) dan mudah lepas dari matriks (die) (Kumoro, 2015).
Cara pembuatan tablet dibagi menjadi tiga cara yaitu
granulasi basah, granulasi kering (mesin rol atau mesin slug) dan kempa
langsung.
a.
Granulasi basah
Granulasi basah dilakukan dengan mencampurkan zat
khasiat, zat pengisi, dan zat penghancur sampai homongen lalu dibasahi dengan
larutan bahan pengikat. Setelah itu diayak menjadi granul dan dikeringkan dalam
lemari pengering pada suhu 40-500C (tidak lebih dari 600C). Setelah kering
diayak lagi untuk memperoleh granuldengan ukuran yang diperlukan dan
ditambahkan bahan pelicin kemudian dicetak menjadi tablet dengan mesin tablet.
Cara granulasi basah menghasilkan tablet
yang lebih baikdan dapat disimpan lebih lama dibanding granulasi kering (Kumoro,
2015).
Keuntungan metode granulasi basah, yaitu:
1)
Meningkatkan kohesifitas dan
kompaktibilitas serbuk sehingga diharapkan tablet yang dibuat dengan mengempa
sejumlah granul pada tekanan kompresi tertentu akan menjadi massa yang kompak,
mempunyai penampilan, cukup keras dan tidak rapuh.
2)
Untuk obat dengan kompaktibilitas
rendah, dalam takaran tinggi dibuat dengan metode ini tidak perlu bahan
penolong yang menyebabkan bobot tablet lebih besar.
3)
Sistem granulasi basah mencegah
terjadinya segregasi komponen penyusun tablet yang homogen selama proses
pencampuran.
4)
Untuk hidrofob maka granulasi
basah dapat memperbaiki kecepatan pelarutan obat (Supriyanti, 2014)
b.
Granulasi kering
Granulasi kering dilakukan dengan mencampurkan zat
khasiat, zat pengisi dan zat penghancur serta jika perlu ditambahkan zat
pengikat dan zat pelicin hingga menjadi serbuk yang homongen, lalu dikempa
cetak pada tekanan tinggi sehingga menjadi tablet besar (slug) yang tidak
berbentuk baik, kemudian digiling dan diayak hingga diperoleh granul dengan
ukuran partikel yang diinginkan. Akhirnya dikempa cetak lagi sesuai ukuran
tablet yang diinginkan (Kumoro, 2015).
c.
Cetak langsung
Cetak atau kempa langsung dilakukan jika: Jumlah zat
khasiat per tabletnya cukup untuk dicetak, zat khasiatnya mempunyai sifat alir
yang baik dan zat khasiat berbentuk kristal yang bersifatfree-flowing (Kumoro,
2015).
Keuntungan penggunaan metode ini adalah waktu produksi
yang lebih singkat, dapat dipakai untuk bahan yang tidak tahan air, tetapi
kerugiannya adalah sering terjadi pemisahan antar partikel (segregasi) pada
waktu partikel turun di hopper ke die sehingga terjadi ketidakseragaman bahan
aktif (Supriyanti, 2014).
4.
Uraian Bahan Pengikat
1)
Gelatin
Gelatin merupakan pengikat yang baik. Larutan gelatin
harus digunakan panas untuk mencegah terbentuknysa gel. Dalam penelitian
ditunjukkan bahwa peningkatan kandungan gelatin dalam tablet menyebabkan
peningkatan waktu hancur dan memperlambat laju disolusi. Larutan gelatin dibuat
dengan membiarkan gelatin terhidrasi dalam air dingin untuk beberapa jam,
kemudian campuran dipanaskan sampai mendidih. Larutan gelatin harus dibiarkan
panas hingga selesai digunakan sebab larutan akan membentuk gel dalam keadaan
dingin. Larutan gelatin cenderung menghasilkan tablet yang memerlukan
disintegran aktif (Allen, 2014).
2)
Polivinilpirolidon (PVP)
PVP telah menjadi pengikat polimer serbaguna. PVP
merupakan zat larut alkohol yang digunakan dalam konsentrasi 3 sampai 5%.
Granulasi yang menggunakan sistem PVP-alkohol dapat diproses dengan baik, cepat
kering, dan sifat kempa sangat baik. PVP sedikit higroskopis, tablet yang
dibuat dengan PVP biasanya tidak menjadi keras seiring bertambahnya waktu dan
membuatnya menjadi suatu pengikat yang baik untuk tablet kunyah (Allen, 2014).
PVP merupakan salah satu bahan tambahan farmasi yang
biasanya digunakan sebagai bahan desintegran, agen pensuspensi, bahan tambahan
granulasi dan sebagai bahan pengikat tablet baik dalam cetak langsung maupun
granulasi basah.
3)
Amilum manihot
Amilum merupakan suatu bahan tambahan farmasi yang biasa
digunakan sebagai bahan pengembang, pengering, serta bahan pengikat pada tablet
maupun kapsul. Penggunaannya sebagai diluen pati digunakan untuk persiapan pada
ekstrak herbal dan memfasilitasi pencampuran pada proses formulasi.
Penggunaannya sebagai lubrikan jumlah amilum yang digunakan biasanya 3-10%,
sedangkan pada pembuatan pasta amilum sebagai pengikat granulasi basah tablet
biasanya digunakan pada konsentrasi 3-20% (tergantung pada tipe amilum) dan
sebagai desintegran biasanya digunakan pada konsentrasi 3-25%.
D.
Alat dan Bahan
Alat-alat yang
digunakan adalah pisau, lemari pengering, kertas perkamen, lampu, neraca kasar,
neraca listrik, blender, corong, kurs porselin, talam, kertas saring, penjepit
tabung, cawan porselin, gelas ukur, erlenmeyer,
thermometer, pipet tetes, ayakan mesh nomor 12, ayakan mesh nomor 16, ayakan
mesh nomor 20, ayakan mesh nomor 40, ayakan mesh nomor 100, lumpang dan alu,
beaker glass, seperangkat alat destilasi penetapan kadar air, stopwatch, spatel, mesin cetak tablet, Roche friabilator, hardness tester (Copley) dan alat-alat gelas lainnya.
Bahan-bahan
yang digunakan pada penelitian ini adalah jahe merah (Zingiber officinale Roxb), etanol 96%, aquadest, kloralhidrat,
toluen, air, asam klorida 2N, asam klorida 3N, Na sulfat anhidrat, timbal (II)
asetat, FeCl3 10%, isopropanol, asam asetat glasial, pereaksi Meyer,
pereaksi Bouchardat, pereaksi
Dragendorff,
pereaksi Molisch, ekstrak kering jahe merah, klorofom, corn starch, laktosa, amylum manihot, gelatin, PVP, Mg stearat,
talcum dan vitamin B6.
E.
Prosedur Kerja
1.
Pengambilan sampel
Teknik
pengambilan sampel adalah purposive sampling yaitu sampel yang dipilih secara
khusus berdasarkan tujuan penelitian. Sampel yang digunakan adalah jahe merah
yang diambil dari Pematang Raya, Kabupaten Simalungun, Sumatera Utara.
2.
Identifikasi sampel
Identifikasi
tanaman dilakukan di Laboratorium Herbarium Medanese, Universitas Sumatera
Utara, Medan.
3.
Pembuatan simplisia
Jahe merah
segar dicuci kemudian disortasi basah, ditiriskan dan ditimbang. Jahe merah
dirajang dengan ketebalan 1-3 mm, lalu dikeringkan dalam lemari pengering pada
temperature + 400C. Jahe merah yang telah kering ditandai dengan rapuh saat dipatahkan dan mempunyai
berat konstan. Simplisia diserbuk dengan blender dan disimpan dalam wadah
plastik bertutup (BPOM RI, 2014)
F.
Karakterisasi Simplisia
Karakterisasi
simplisia meliputi pemeriksaan makroskopik dan mikroskopik, penetapan kadar abu
total, penetapan kadar abu larut asam, penetapan kadar sari larut dalam air,
penetapan kadar sari larut dalam etanol dan penetapan kadar air.
1.
Pemeriksaan makroskopik
Pemeriksaan
makroskopik dilakukan dengan mengamati morfologi jahe merah dengan cara
memperhatikan warna, bentuk, ukuran, dan tekstur dari jahe merah.
2.
Pemeriksaan mikroskopik
Pemeriksaan mikroskopik terhadap simplisia dilakukan dengan cara menaburkan serbuk simplisia diatas kaca objek yang telah diteteskan dengan kloralhidrat dan ditutup dengan kaca penutup kemudian dilihat dibawah mikroskop dan untuk pati dilihat dalam aquadest.
Lebih kurang 2
g sampai 3 g zat yang telah digerus dan ditimbang seksama, masukkan kedalam
krus platina atau krus silikat yang telah dipijarkan dan ditara, ratakan.
Pijarkan perlahan-lahan hingga arang habis, dinginkan, timbang. Dengan cara ini
arang tidak dapat dihilangkan, tambahkan air panas, saring melalui kertas
saring bebas abu. Pijarkan sisa dan kertas saring dalam krus yang sama.
Masukkan filtrat ke dalam krus,
uapkan, pijarkan hingga bobot tetap, timbang. Hitung kadar abu terhadap bahan
yang telah dikeringkan di udara (BPOM RI, 2014)
4.
Penetapan kadar abu yang tidak
larut dalam asam
Abu yang
diperoleh pada penetapan kadar abu, didihkan dengan 25 ml asam klorida encer
selama 5 menit, kumpulkan bagian yang tidak larut dalam asam, saring melalui
krus kaca masir atau kertas saring bebas abu, cuci dengan air panas, pijarkan
hingga bobot tetap, timbang. Hitung kadar abu yang tidak larut dalam asam
terhadap bahan yang telah dikeringkan di udara (BPOM RI, 2014)
5.
Penetapan kadar sari yang larut
dalam air
Keringkan
serbuk di udara, maserasi selama 24 jam 5,0 g serbuk dengan 100 ml air
kloroform, menggunakan labu bersumbat sambil berkali-kali dikocok selama 6 jam
pertama dan kemudian dibiarkan selama 18 jam. Saring dan uapkan 20 ml filtrat
hingga kering dalam cawan dangkal berdasar rata yang telah ditara, panaskan
sisa pada suhu 1050C hingga bobot tetap. Hitung kadar dalam persen
sari yang larut dalam air, dihitung terhadap bahan yang telah dikeringkan di
udara (BPOM RI, 2014)
6.
Penetapan kadar sari yang larut
dalam etanol
Keringkan
serbuk di udara, maserasi selama 24 jam 5,0 g serbuk dengan 100 ml etanol
(95%), menggunakan labu bersumbat sambil berkali-kali dikocok selama 6 jam
pertama dan kemudian dibiarkan selama 18 jam. Saring cepat dengan menghindarkan
penguapan etanol (95%), uapkan 20 ml filtrat hingga kering dalam cawan dangkal
berdasar rata yang telah ditara, panaskan sisa pada suhu 1050C
hingga bobot tetap. Hitung kadar dalam persen sari yang larut dalam etanol
(95%), dihitung terhadap bahan yang telah dikeringkan diudara (BPOM RI, 2014)
Penetapan
kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Alat terdiri
dari labu alas bulat 500 ml, alat penampung, pendingin, tabung penyambung dan
tabung penerima. Cara penetapannya, yaitu: Pada labu bulat dimasukkan 200 ml
toluena dan 2 ml air suling, didestilasi selama 2 jam. Destilasi dihentikan dan
dibiarkan dingin selama 30 menit, kemudian volume air di dalam tabung penerima
dibaca dengan ketelitian 0,05 ml. Labu yang berisi toluen jenuh tersebut
dimasukkan 5 g serbuk simplisia yang telah ditimbang saksama, lalu dipanaskan hati-hati selama 15 menit, setelah
toluene mulai mendidih, kecepatan tetesan diatur lebih kurang 2 tetes per detik
hingga sebagian air tersuling. Kecepatan dinaikkan hingga 4 tetes per detik,
kemudian setelah semua air tersuling, bagian dalam pendingin dibilas dengan
toluena. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima
dibiarkan mendingin sampai suhu kamar, setelah air dan toluen memisah sempurna,
volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca
sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air
dihitung dalam persen.
G.
Pembuatan Ekstrak Jahe Merah
Pembuatan
ekstrak jahe merah dilakukan dengan cara maserasi. Maserasi dilakukan dengan
cara 10 bagian simplisia atau campuran simplisia dengan derajat halus yang cocok kedalam sebuah
bejana, tuangi dengan 75 bagian cairan penyari (etanol 96%), tutup dan biarkan
selama 5 hari terlindung dari cahaya sambil sering diaduk, serkai, peras, cuci
ampas dengan cairan penyari (etanol 96%) secukupnya hingga diperoleh 100
bagian. Pindahkan kedalam bejana tertutup, biarkan ditempat sejuk, terlindung
dari cahaya, selama 2 hari. Enap tuangkan atau saring, dipekatkan dengan
penguapan dan tekanan pada suhu rendah 50oC hingga konsentrasi yang
dikehendaki (BPOM RI, 2014)
Gambar. Flowchart pembuatan Jahe Merah
H.
Skrining Fitokimia
Skrining
fitokimia adalah metode analisis untuk menentukan jenis metabolit sekunder yang
terdapat dalam tumbuh-tumbuhan karena sifatnya yang dapat bereaksi secara khas
dengan pereaksi tertentu. Skrining fitokimia dilakukan melalui serangkaian pengujian dengan
menggunakan pereaksi tertentu. Pada percobaan ini uji yang dilakukan yaitu uji
steroid/triterpenoid, uji alkaloid, uji flavonoid, uji saponin, uji tanin, uji
glikosida.
Pereaksi
Lieberman-Burchard adalah pereaksi yang sering digunakan untuk uji senyawa
terpenoid. Pereaksi ini dibuat dari campuran anhidrid asetat dan H2SO4
pekat. Kebanyakan triterpena dan sterol memberikan warna hijau biru dengan
pereaksi ini. Cara lain untuk mendeteksi terpena adalah menyemprot plat KLT
dengan larutan KMnO4 0,2% dalam air, antimon dalam kloroform, H2SO4
pekat atau vanillin-H2SO4. Setelah penyemprotan, senyawa
yang positif mengandung terpenoid akan menunjukkan perubahan warna (Saparinto,
2016).
Timbang 0,5 g
ekstrak jahe merah, tambahkan 1 ml asam klorida 2 N dan 9 ml air, panaskan
diatas penangas air selama 2 menit, dinginkan dan saring.
1)
Pindahkan 3 tetes filtrat
pada tabung reaksi,
tambahkan 2 tetes Bouchardat.
2)
Jika pada
percobaan tidak terjadi endapan, maka serbuk tidak mengandung alkaloid.
3)
Pindahkan 3 tetes filtrat
tambahkan 2 tetes pereaksi Mayer. Jika terbentuk endapan berwarna putih atau
kuning yang larut dalam methanol, maka kemungkinan terdapat alkaloid.
4)
Pindahkan 3 tetes filtrat
tambahkan 2 tetes pereaksi Dragendorff, akan terbentuk endapan berwarna merah
sampai coklat jika mengandung alkaloida.
Ekstrak
mengandung alkaloid jika sekurang-kurangnya terbentuk endapan dengan
menggunakan dua golongan larutan percobaan yang digunakan (BPOM RI, 2014)
Ekstrak jahe
merah sebanyak 0,5 g ditambahkan 10 ml methanol, direfluks selama 10 menit. Saring
panas melalui kertas saring berlipat. Encerkan filtrat dengan 10 ml air.
Setelah dingin tambahkan 5 ml eter minyak tanah, kocok hati- hati diamkan.
Ambil lapisan metanol, uapkan pada suhu 400C. Sisa dilarutkan dalam
5 ml etil asetat, saring.
1)
Pindahkan sebanyak 1 ml filtrat
diuapkan sampai kering, sisa dilarutkan dalam 1 ml sampai 2 ml etanol (95%),
tambahkan 0,5 g serbuk seng dan 2 ml asam klorida 2 N, diamkan selama 1 menit.
Tambahkan 10 tetes asam klorida pekat. Jika dalam waktu 2-5 menit terjadi warna
merah intensif, menunjukkan adanya flavonoid.
2)
Pindahkan 1 ml filtrat diuapkan
hingga kering, sisa dilarutkan dalam 1 ml etanol (95%), tambahkan 0,1 g serbuk
magnesium dan 10 tetes asam klorida pekat, jika terjadi warna merah jingga
sampai merah ungu, menunujukkan adanya flavonoid.
3)
Pindahkan 1 ml filtrat diuapkan
hingga kering, basahkan sisa dengan aseton, tambahkan sedikit serbuk halus asam
borat dan serbuk halus asam okasalat, panaskan hati-hati diatas penangas air.
Campur sisa yang diperoleh dengan 10 ml eter. Amati dengan sinar UV 366 nm;
larutan berfluoresensi kuning intensif, menunjukkan adanya flavonoid (BPOM RI,
2014)
Sebanyak 0,5 g
ekstrak jahe merah dimasukkan kedalam tabung reaksi, tambahkan 10 ml air panas,
dinginkan dan kemudian kocok kuat-kuat selama 10 detik. Terbentuk buih yang
mantap selama tidak kurang 10 menit, setinggi 1 cmsampai 10 cm. Penambahan 1
tetes asam klorida 2 N, buih tidak hilang (BPOM RI, 2014)
Ekstrak jahe
merah sebanyak 500 mg, dipanaskan dengan 10 ml air, disaring, diencerkan sampai
hampir tidak berwarna. Pada 2 ml larutan sampel ditambahkan 1-2 tetes larutan
FeCl3 10%, diperhatikan warna yang terjadi, warna biru atau hijau
kehitaman menandakan adanya tanin (BPOM RI, 2014).
Ekstrak jahe
merah sebanyak 3 g dicampurkan dengan 30 mL campuran
7 bagian etanol 96% dan 3 bagian air, ditambahkan 10 ml asam sulfat 2N, lalu
direfluks selama 10 menit, didinginkan dan disaring. Filtrat sebanyak 20 ml
tambahkan 25 ml air dan 25 ml larutan timbal (II) asetat 0,4 M, dikocok dan
didiamkan selama 5 menit lalu disaring. Filtrat disari 3 kali dan tiap kali
dengan 20 ml campuran 3 bagian kloroform dan 2 bagian isopropanol, pada
kumpulan sari ditambahkan natrium sulfat anhidrat pekat lalu disaring dan diuapkan
pada suhu tidak lebih dari 50oC. Sisa dilarutkan dengan 2 ml metanol
pekat. Larutan sisa digunakan untuk percobaan berikut: Larutan sebanyak 5 tetes
dimasukkan dalam tabung reaksi, lalu ditambahkan 2 ml air dan 5 tetes pereaksi
Molisch, kemudian ditambahkan dengan hati-hati 2 ml asam sulfat pekat hingga
terbentuk cincin berwarna ungu pada batas cairan, menunjukkan adanya ikatan
gula (BPOM RI, 2014).
I.
Pengenceran Ekstrak
Ekstrak kental
jahe merah yang diperoleh diencerkan dengan penambahan amylum manihot dengan
perbandingan ekstrak kental jahe merah dan amylummanihot 1:3, kemudian digerus
sampai homogen. Sampai diperoleh sediaanserbuk. Diayak dengan ayakan mesh nomor
40 lalu dikeringkan dengan lemari pengering sampai massa kering.
J.
Uji Preformulasi
Uji preformulasi yang dilakukan adalah
penentuan sudut diam, penentuan waktu alir granul dan penentuan indeks tap.
1.
Sudut diam granul
Tiap formula dituang pelan-pelan lewat
corong, sementara bagian bawah corong ditutup, kemudian penutup dibuka dan
granul dibiarkan mengalir keluar. Diukur tinggi dan jari-jari kerucut yang
terbentuk, kemudian ditentukan sudut diamnya. Granul yang mempunyai daya alir
bebas akan mempunyai sudut diam antara 20o – 40o .
2.
Penetapan waktu alir granul
Granul yang akan dicetak dimasukkan kedalam
corong alir, lalu dialirkan hingga seluruh granul mengalir. Waktu alir
ditentukan hingga seluruh formula mengalir keluar. Syarat waktu alir yang baik
adalah kurang dari 10 detik.
Penentuan indeks tap
dilakukan dengan cara: Granul dimasukkan ke dalam gelas ukur sampai garis tanda
dan dinyatakan sebagai volume awalnya (V1), kemudian gelas ukur dihentakkan
sebanyak 20 kali dengan alat yang dimodifikasi sehingga diperoleh volume akhir
(V2).
K.
Formula Pembuatan Tablet
Dasar
pemilihan dosis untuk membuat tablet jahe merah diambil berdasarkan sediaan
kapsul vitamam I yang mengandung zat aktif jahe merah dengan dosis sebesar 0,2
g dan vitamin B6 0,015 g. Aturan pemakaian kapsul vitamam I yaitu 1x1.
Berdasarkan orientasi yang dilakukan dengan dosis 0,2 g tablet tidak dapat
dicetak maka untuk memenuhi dosis ekstrak kental jahe merah yang digunakan
yaitu 0,067 g dan vitamin B6 0,005 g dengan aturan pemakaian dibuat menjadi
1x3. Proses pembuatan tablet jahe merah sebagai zat aktif menggunakan metode
granulasi basah sebanyak 9 formula yang masing-masing terdiri dari 50 tablet.
Perbedaan dari 9 formula adalah jenis bahan pengikat dengan konsentrasi yang
divariasikan yaitu Gelatin (10%, 12,5%, 15%), Amylum manihot (7,5%, 10%, 12,5%)
dan PVP (2%, 4%, 6%).
R/ Ekstrak jahe merah 0, 268
Vitamin B6 0,005
Corn Starch 5%
Bahan pengikat
(variasi) x Talkum 1%
Mg stearat 2%
Laktosa ad 0,650
m.f.tab dtd No L Bobot per tablet: 650 mg
Diameter: 13 mm
Tabel 3.1 Formula tablet ekstrak jahe merah dengan beberapa
bahan pengikat
|
Bahan |
Formula |
||||||||
|
F1 |
F2 |
F3 |
F4 |
F5 |
F6 |
F7 |
F8 |
F9 |
|
|
Ekstrak jahe merah |
13,4 |
13,4 |
13,4 |
13,4 |
13,4 |
13,4 |
13,4 |
13,4 |
13,4 |
|
Vitamin B6 |
0,250 |
0,250 |
0,250 |
0,250 |
0,250 |
0,250 |
0,250 |
0,250 |
0,250 |
|
Amylum |
0,731 |
0,975 |
1,219 |
- |
- |
- |
- |
- |
- |
|
Gelatin |
- |
- |
- |
0,975 |
1,219 |
1,463 |
- |
- |
- |
|
PVP |
- |
- |
- |
- |
- |
- |
0,650 |
1,3 |
1,950 |
|
Corn starch |
1,625 |
1,625 |
1,625 |
1,625 |
1,625 |
1,625 |
1,625 |
1,625 |
1,625 |
|
Talkum |
0,325 |
0,325 |
0,325 |
0,325 |
0,325 |
0,325 |
0,325 |
0,325 |
0,325 |
|
Mg stearate |
0,650 |
0,650 |
0,650 |
0,650 |
0,650 |
0,650 |
0,650 |
0,650 |
0,650 |
|
Laktosa |
519 |
15,275 |
15,031 |
15,275 |
15,031 |
14,747 |
15,600 |
14,950 |
14,300 |
Keterangan:
F1:Formula tablet ekstrak jahe merah dengan konsentrasi amilum manihot 7,5%
F2:Formula tablet ekstrak jahe merah dengan
konsentrasi amilum manihot 10% F3:Formula tablet ekstrak jahe merah dengan konsentrasi amilum manihot 12,5%
F4:Formula tablet ekstrak jahe merah dengan
konsentrasi gelatin 10%
F5:Formula tablet ekstrak jahe merah dengan konsentrasi gelatin 12,5%
F6:Formula tablet ekstrak jahe merah dengan konsentrasi gelatin 15%
F7:Formula tablet ekstrak jahe merah dengan konsentrasi PVP 2%
F8:Formula tablet ekstrak jahe merah dengan konsentrasi PVP 4%
F9:Formula tablet ekstrak jahe merah dengan konsentrasi PVP 6%
1.
Pembuatan tablet ekstrak jahe
merah
Tablet ekstrak
jahe merah dibuat dengan metode granulasi basah dengan beberapa macam bahan
pengikat dengan konsentrasi yang divariasi dilakukan dengan cara:
1)
Alat-alat yang digunakan
dibersihkan dan ditimbang semua bahan yang digunakan.
2)
Laktosa dimasukkan kedalam lumpang
dan digerus, ditambahkan vitamin B6 dan
Corn starch
3)
Ekstrak jahe merah ditambahkan
kedalam lumpang dan digerus homogen
4)
Masing-masing bahan pengikat
dibuat dengan konsentrasi yang telah ditentukan.
5)
Pengikat yang telah dibuat
ditambahkan sedikit demi sedikit kedalam lumpang hingga terbentuk massa yang
kompak.
6)
Massa yang kompak diayak dengan
ayakan mesh nomor 14 dan dikeringkan
7)
Massa yang kering diayak kembali
dengan ayakan mesh nomor 16
8)
Talkum dan Mg stearat ditambahkan
kedalam granul yang kering dan
dilakukan uji preformulasi
9)
Tablet dapat dicetak dan dilakukan
uji evaluasi (Lette,
2016).
L.
Evaluasi Tablet
Evaluasi
tablet yang dilakukan adalah keseragaman bobot, kekerasan tablet, friabilitas
dan waktu hancur.
1.
Keseragaman bobot
Penetapan
keseragaman bobot menggunakan neraca analitik Boeco. Tablet tidak bersalut
harus memenuhi syarat keseragaman bobot yang ditetapkan sebagai berikut:
Timbang 20 tablet, hitung bobot rata-rata tiap tablet. Jika ditimbang satu
persatu, tidak boleh lebih dari 2 tablet yang masing-masing bobotnya menyimpang
dari bobot rata-ratanya lebih besar dari harga yang ditetapkan kolom A, dan tidak satu tablet pun yang bobotnya
menyimpang dari bobot rata-ratanya lebih dari harga yang ditetapkan kolom B.
Jika tidak mencukupi 20 tablet, dapat digunakan
10 tablet; tidak satu tablet pun yang bobotnya menyimpang lebih besar dari
bobot rata-rata yang ditetapkan kolom A dan tidak satu tablet pun yang bobotnya
menyimpang lebih besar dari bobot rata- rata yang ditetapkan kolom B (BPOM RI,
2014)
Tabel 3.2 Syarat Penyimpangan Bobot
|
Bobot rata –
rata |
Penyimpangan
bobot rata – rata dalam % |
|
|
A |
B |
|
|
25 mg atau kurang |
15% |
30% |
|
26 mg sampai dengan 150 mg |
10% |
20% |
|
151 mg sampai dengan 300 mg |
7,5% |
15% |
|
Lebih dari 300 mg |
5% |
10% |
Penetapan
friabilitas tablet menggunakan alat Roche friabilator. Tablet yang akan diuji
sebanyak 20 tablet. Ditimbang 20 tablet yang telah dibersihkan dari debu (A)
dimasukkan ke dalam alat dan diputar selama 4 menit. Tablet dikeluarkan dan
dibersihkan dari debu kemudian ditimbang (B), kehilangan bobot tidak lebih dari
0,8 % (Banker dan Anderson, 1994).
3.
Uji kekerasan
Penetapan
kekerasan tablet menggunakan alat Strong cobb hardness tester. Tablet yang akan
diuji sebanyak 5 tablet. Diletakkan sebuah tablet antara anvil dan punch tegak
lurus, tablet dijepit dengan cara memutar skrup pemutar sampai lampu stop
menyala. Skrup ditekan dan dicatat angka yang ditunjukkan jarum penunjuk skala
pada saat tablet pecah. Percobaan ini dilakukan untuk 5 tablet. Syarat kekerasan
tablet 4 kg–8 kg (Kumoro, 2015).
4.
Waktu hancur
Alat:
disintegrator tester. Alat terdiri dari suatu rangkaian keranjang, gelas piala
berukuran 100 ml termostat dengan suhu 36-38°C dan alat untuk menaik turunkan
keranjang dengan frekuensi 29-32 kali permenit. Cara: satu tablet dimasukkan
kedalam masing-masing tabung dari keranjang, dimasukkan satu cakram pada tiap
tabung dan dijalankan, sebagai media digunakan air suling dengan suhu 37± 2°C.
Pada akhir batas waktu dinyatakan sebagai waktu hancur tablet, yaitu waktu
dimana semua bagian tablet telah melewati kawat kasa. Pengujian dengan 6
tablet, dimana selama 15 menit seluruh tablet telah hancur dan melewati kasa
pada tabung (Lette, 2016).
BAB III
HASIL DAN PEMBAHASAN
A.
Hasil Identifikasi Tumbuhan
Tumbuhan yang
digunakan diidentifikasi di Laboratorium Herbarium Medanase, Universitas
Sumatera Utara. Hasil identifikasi tumbuhan yang dikirim adalah jahe merah dari
famili Zingiberaceae (Lette, 2016).
B.
Hasil Pengolahan Sampel
Hasil
pengolahan jahe merah yang masih segar dicuci kemudian disortasi basah,
ditiriskan dan ditimbang. Jahe merah dirajang dengan ketebalan 1-3 mm, lalu
dikeringkan dalam lemari pengering pada temperatur ±40°C. Jahe merah yang telah kering ditandai dengan rapuh saat
di patahkan dan mempunyai berat konstan. Simplisia diserbuk dengan blender,
disimpan dalam wadah plastik bertutup.
C.
Hasil Uji Karakterisasi Simplisia
1.
Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik dari simplisia jahe merah yaitu menunjukkan
berbentuk bulat memanjang, keras, warna merah, warna daging kecoklatan, panjang
3-4 cm, permukaan luar berkerut, melengkung tidak beraturan, tidak rata, bau
khas, rasa pedas (Lette, 2016).
2.
Hasil pemeriksaan mikroskopik
Hasil uji karakterisasi simplisia jahe merah
dpat dilihat pada tabel 4.1.
Tabel 4.1 Hasil uji karakterisasi simplisia jahe merah
|
Karakteristik |
Hasil pemeriksaan |
Depkes RI, |
1978 (%) |
|
Kadar air |
3,994 |
Maks 10 |
|
|
Kadar sari larut air |
16,17 |
≥ 15,6 |
|
|
Kadar sari larut etanol |
17,28 |
≥ 4,3 |
|
|
Kadar abu total |
3,806 |
≤ 5 |
|
|
Kadar abu tidak larut asam |
2,511 |
≤ 3,9 |
|
Hasil
penetapan kadar air yang terkandung dalam simplisia jahe merah yaitu 3,994 %
dan memenuhi persyaratan dari buku Materia Medika Indonesia yaitu tidak lebih
dari 10%. Kadar air yang tinggi akan menyebabkan bahan menjadi rusak ketika
disimpan karena adanya pertumbuhan mikroba dan hidrolisis senyawa kimia.
Penetapan kadar sari larut etanol dan penetapan kadar sari larut air adalah
17,28% dan 16,17% nilai tersebut sesuai dengan kriteria mutu yang ditentukan
tidak kurang dari 15,6% dan tidak kurang dari 4,3 %. Penetapan kadar sari yang
larut dalam air dan etanol dilakukan untuk mengetahui adanya zat berkhasiat
yang dapat terlarut dalam pelarut yang digunakan. Semakin tinggi kadar yang
dihasilkan berarti semakin tinggi kandungan zat berkhasiatnya (Gaman dan Sherington,
1992). Senyawa- senyawa yang dapat larut dalam air adalah glikosida, gula, gom,
protein, enzim, zat warna dan asam organik.
Senyawa-senyawa yang dapat larut dalam etanol adalah glikosida, antrakinon,
steroid terikat, klorofil, dan dalam jumlah sedikit yang larut yaitu lemak dan
saponin (BPOM RI, 2014).
Penetapan
kadar abu total untuk mengetahui kadar zat anorganik yang terdapat pada
simplisia, sedangkan penetapan kadar abu tidak larut asam untuk mengetahui
kadar zat anorganik yang tidak larut dalam asam (BPOM RI, 2014).
D.
Hasil Ekstraksi Jahe Merah
Hasil
penyarian 2,6 kg serbuk simplisia jahe merah dengan pelarut etanol 96% dengan
perbandingan antara serbuk dan pelarut yaitu 1:10, diperoleh ekstrak cair yang
kemudian diuapkan dengan menggunakan rotary evaporator, diperoleh ekstrak
kental sebanyak 418,46 g dengan persen rendemen 16,095 %. Ekstrak inilah yang
digunakan sebagai bahan formulasi sediaan tablet.
E.
Hasil Skrining Fitokimia
Hasil skrining
fitokimia terhadap ekstrak jahe merah dapat dilihat pada Tabel 4.2
Tabel 4.2 Hasil skrining
fitokimia ekstrak jahe merah
|
Golongan senyawa kimia |
Hasil |
|
Alkaloid |
- |
|
Flavonoid |
+ |
|
Tanin |
+ |
|
Saponin |
+ |
|
Triterpenoid |
+ |
|
Glikosida |
+ |
Keterangan:
(+) =
Mengandung senyawa
(–) =
Tidak mengandung senyawa
UJi skrining fitokimia
dilakukan untuk mengetahui senyawa kimia yang terkandung pada ekstrak jahe
merah. Berdasarkan penelitian yang dilakukan bahwa ekstrak jahe merah memiliki
golongan senyawa flavonoid, tanin, saponin, steroid/triterpenoid dan glikosida.
Hasil skrining ekstrak jahe merah menunjukkan adanya saponin dengan
terbentuknya buih yang stabil, flavonoid ditunjukkan dengan warna merah
intensif.
F.
Hasil Uji Preformulasi
1.
Waktu alir granul
Hasil uji
waktu alir granul dari 9 formula dengan metode granulasi basah dapat dilihat
pada Tabel 4.3.
Tabel 4.3 Hasil uji
waktu alir granul dari 9 formula
|
Formula |
Uji preformulasi |
Persyaratan |
|
Waktu alir |
||
|
F1 |
4,05 |
<10 detik |
|
F2 |
4,21 |
|
|
F3 |
4,49 |
|
|
F4 |
3,64 |
|
|
F5 |
3,89 |
|
|
F6 |
3,89 |
|
|
F7 |
5,14 |
|
|
F8 |
6,15 |
|
|
F9 |
6,40 |
Berdasarkan data
yang diperoleh bahwa uji waktu alir granul memenuhi persyaratan yaitu tidak
lebih dari 10 detik. Apabila waktu yang diperlukan oleh 100 g granul untuk
mengalir keluar dari corong lebih dari 10 detik, akan mengalami kesulitan waktu
penabletan (Lestari dan Natalia, 2007)
Gambar 4.1 Histogram Waktu Alir Granul
Uji waktu alir granul dari setiap formula berbeda- beda sesuai dengan
konsentrasi pengikat yang digunakan, pada
formula F4-F6 waktu alir granul lebih cepat dibandingkan dengan waktu alir
granul pada formula F1-F3, dan F7-F9. Kecepatan alir
dipengaruhi oleh bentuk, ukuran, kondisi permukaan, kelembapan granul dan
penambahan bahan pelicin. Analitik granul mempunyai sifat alir yang baik maka
pengisian pada ruang kempa menjadi konstan sehingga dihasilkan tablet yang
mempunyai bobot seragam (Kumoro, 2015). Ukuran granul pada formula F4-F6 lebih
besar dibandingkan dengan formula F1-F3 dan F7-F9. Hasil pengujian distribusi
partikel bahwa granul yang dihasilkan oleh formula menggunakan gelatin lebih
banyak dibandingkan formula menggunakan amylum dan PVP. Ukuran partikel granul
makin kecil akan memperbesar gaya kohesinya sehingga granul akan menggumpal dan
menghambat kecepatan alirannya.
2.
Hasil uji sudut diam
Hasil uji
sudut diat granul dari 9 formula dengan metode granulasi basah dapat dilihat
pada Tabel 4.4
Tabel 4.4 Hasil uji sudut diam dari 9
formula
|
Formula |
Uji preformulasi |
Persyaratan |
|
Sudut diam (0) |
||
|
F1 |
25,174 |
200-400 |
|
F2 |
29,726 |
|
|
F3 |
26,151 |
|
|
F4 |
27,203 |
|
|
F5 |
27,203 |
|
|
F6 |
26,151 |
|
|
F7 |
23,509 |
|
|
F8 |
23,509 |
|
|
F9 |
19,188 |
Metode sudut diam digunakan sebagai metode tidak langsung untuk mengukur
mampu alir serbuk karena hubungannya dengan kohesi antarpartikel.Suatu serbuk
yang tidak kohesif mengalir baik, menyebar, membentuk timbunan yang rendah. Bahan yang kohesif membentuk timbunan yang
lebih tinggi yang kurang menyebar (Allen, 2014).
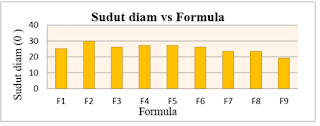
Gambar 4.2 Histogram Sudut Diam Granul
Berdasarkan
gambar uji preformulasi sudut diam dari formula F1-F9, memenuhi persyaratan
yaitu antara 200- 400. Bila sudut baring lebih kecil atau
sama dengan 300 biasanya menunjukkan bahwa bahan dapat mengalir
bebas, bila sudutnya lebih besar atau sama dengan 400 biasanya daya
mengalirnya kurang baik. Dari nilai sudut diam dan kompresibilitas dapat
menunujukkan indikasi bias diterimanya sifat aliran yang dimiliki suatu bahan
(Kumoro, 2015).
3.
Hasil uji indeks tap granul
Hasil uji
indeks tap granul dari 9 formula dengan metode granulasi basah dapat dilihat
pada Tabel 4.5.
Tabel 4.5 Hasil Uji
Indeks Tap Granul dari 9 Formula
|
Formula |
Uji preformulasi |
Persyaratan |
|
Indeks tap % |
||
|
F1 |
11,11 |
≤ 20% |
|
F2 |
11,11 |
|
|
F3 |
11,11 |
|
|
F4 |
8,696 |
|
|
F5 |
11,11 |
|
|
F6 |
8,696 |
|
|
F7 |
13,636 |
|
|
F8 |
13,636 |
|
|
F9 |
8,696 |
Kerapatan
granul dapat mempengaruhi kompresibilitas, porositas tablet, kelarutan dan
sifat-sifat lainnya. Granul yang keras, padat memerlukan kompresi yang lebih
besar untuk menghasilkan kohesi yang kompak, seperti tablet - tablet yang
berpenampilan dapat diterima yang bebas dari granul.
Gambar 4.3 Histogram Indeks Tap Granul
Semakin kecil
nilai indeks tap granul maka volume pemampatan akan semakin besar. Hal ini
disebabkan karena jumlah pemakaian dan bahan pengikat yang digunakan berbeda
sehingga menghasilkan bentuk granul yang berbeda. Dari gambar indeks tap granul
dari beberapa formula bervariasi akan tetapi masih memenuhi persyaratan yaitu ≤
20% (Kumoro, 2015).
G.
Uji Evaluasi Tablet
Pada proses
pencetakan tablet formula F1, F2, F3, F4, F5, F6, F7, F8, F9 semua formula
dapat dicetak menjadi tablet. Evaluasi sediaan tablet yang dilakukan yaitu uji
keseragaman bobot, uji kekerasan tablet, uji friabilitas tablet, dan uji waktu
hancur tablet.
1.
Hasil evaluasi keseragaman bobot
Hasil evaluasi keseragaman bobot tablet dengan variasi pengikat dengan
berbagai konsentrasi dari ke sembilan formula yaitu F1, F2,F3, F4, F5, F6, F7,
F8, F9 memenuhi persyaratan bahwa tidak satu tabletpun yang bobotnya menyimpang
dari persyaratan yang ditetapkan, menurut Farmakope Indonesia Edisi III (1979),
yaitu tidak lebih dua tablet yang masing-masing bobotnya menyimpang dari bobot
rata-rata dari harga yang ditetapkan pada kolom A dan tidak satu tablet yang
menyimpang dari bobot yang ditetapkan pada kolom B menurut Tabel 3.2.
Hasil uji
friabilitas tablet ekstrakjahe merah dengan metode granulasi basah dari 9
formula dapat dilihat pada Tabel 4.6.
Tabel 4.6
Hasil Uji Friabilitas
|
Formula |
Uji evaluasi |
Persyaratan |
|
Friabilitas (%) |
||
|
F1 |
0,857 |
≤ 1% |
|
F2 |
0,832 |
|
|
F3 |
0,822 |
|
|
F4 |
0,656 |
|
|
F5 |
0,640 |
|
|
F6 |
0,607 |
|
|
F7 |
0,755 |
|
|
F8 |
0,744 |
|
|
F9 |
0,701 |
Kehilangan
berat lebih kecil dari 0,5% sampai 1% masih dapat dibenarkan. Bila punch
cembung (terlebih lagi yang sangat cembung) digunakan dalam pembuatan tablet,
apalagi kondisinya kurang baik atau tepi permukaannya sudah aus, maka tablet
yang dihasilkan akan berumbai pada tepinya. Tablet seperti ini derajat/ harga friabilitasnya
akan lebih tinggi dari pada normal, karena jumbai-jumbai itu akan dilepaskan
pada waktu pengujian. Kerenyahan tablet dapat juga dipengaruhi oleh kandungan
air dari granul dan produk akhir. Granul yang sangat kering dan hanya mengandung sedikit sekali persentase
kelembapan, sering menghasilkan lebih banyak tablet renyah daripada granul yang
kadar kelembapanya 2 sampai 4%.
Gambar 4.4 Histogram Friabilitas Tablet
Dari gambar
dapat dilihat friabilitas F1-F9 memenuhi persyaratan. Menurut Siregar dan
Wikarsa (2010), menjelaskan bahwa persyaratan friabilitas yaitu maksimal 1%
untuk sediaan tablet konvensional.
3.
Hasil uji kekerasan tablet
Hasil uji
kekerasan tablet ekstrak rimpang jahe merah dari 9 formula dengan metode granulasi
basah dapat dilihat pada Tabel 4.7.
Tabel 4.7 Hasil UJi Kekerasan Tablet
|
Formula |
Uji evaluasi |
Persyaratan |
|
Kekerasan (Kg) |
||
|
F1 |
0,853 |
4-8 Kg |
|
F2 |
1,017 |
|
|
F3 |
1,210 |
|
|
F4 |
1,963 |
|
|
F5 |
2,197 |
|
|
F6 |
2,490 |
|
|
F7 |
1,447 |
|
|
F8 |
1,673 |
|
|
F9 |
1,813 |
Tablet harus
mempunyai kekuatan atau kekerasan tertentu serta tahan atas kerenyahan agar
dapat bertahan terhadap berbagai guncangan mekanik pada saat pembuatan,
pengepakan dan pengapalan. Kekuatan tablet, seperti juga ketebalannya,
merupakan fungsi dari isi die dan gaya kompresi. Pada penambahan tekanan
kompresi, nilai kekerasan tablet meningkat, sedangkan ketebalan tablet
berkurang. Pelincir dapat mempengaruhi kekerasan tablet bila terlalu pekat atau
pencampurannya terlalu lama (Kumoro, 2015).
Gambar 4.5 Histogram Uji Kekerasan Tablet
Dari gambar
dapat dilihat bahwa kekerasan tablet dari tiap formula yaitu dibawah 4 kg.
Menurut (Parrot,1971), persyaratan yang ditetapkan untuk kekerasan tablet yaitu
4-8 kg. Kekerasan tablet dari tiap formula berbeda-beda sesuai dengan jenis dan
jumlah bahan pengikat yang digunakan. Formula F4-F6 mempunyai kekerasan lebih
tinggi dibandingkan dengan formula F1-F3, dan F7- F9. Formula F7-F9 mempunyai
kekerasan lebih tinggi dibandingkan dengan formula F1-F3. Formula 6 dengan menggunakan
pengikat gelatin menghasilkan kekerasan yang lebih besar dibandingkan semua
formula dengan kekerasan mencapai 2,49 kg.
Berdasarkan
hal tersebut bahan pengikat akan mempengaruhi baik buruknya suatu sediaan
tablet. Amilum sebagai bahan pengikat yaitu menghasilkan tablet yang rapuh
sehingga waktu disintregannya lebih singkat tetapi sulit dikeringkan. PVP
menghasilkan tablet yang tidak keras, dan waktu disintegrasinya cepat tetapi
sedikit higroskopis. Gelatin sebagai bahan pengikat yaitu
dapat digunakan pada senyawa yang sulit diikat, akan tetapi cenderung
menghasilkan tablet yang keras sehingga waktu disintegrannya membutuhkan waktu
yang lama selain itu rentan terhadap mikroba. Kekerasan tablet bukanlah
indikator yang absolut dari kekuatan tablet, karena pada beberapa formulasi,
bila dikempa menjadi tablet yang sangat keras, cenderung akan terjadi cap pada
pergesekan, sehingga menghilangkan bagian atas, karena itu cara lain untuk
mengukur kekuatan tablet yaitu friabilitas (Kumoro, 2015).
4.
Hasil uji evaluasi waktu hancur tablet
Hasil uji
evaluasi waktu hancur tablet rimpang jahe merah dari 9 formula dapat dilihat
pada Tabel 4.8.
Tabel 4.8 Hasil Uji Waktu Hancur
|
Formula |
Uji evaluasi |
Persyaratan |
|
Waktu hancur (menit) |
||
|
F1 |
5,33 |
≤ 15 menit |
|
F2 |
6.59 |
|
|
F3 |
7.45 |
|
|
F4 |
9.05 |
|
|
F5 |
12.47 |
|
|
F6 |
14.16 |
|
|
F7 |
6. 09 |
|
|
F8 |
7.12 |
|
|
F9 |
8.52 |
Tablet
dinyatakan hancur jika terlarut dalam suatu medium penguji atau hancur menjadi
banyak partikel. Langkah penting pertama sebelum melarut adalah pecahnya tablet
menjadi partikel kecil atau granul yang disebut disentegrasi (Kumoro, 2015).
Gambar 4.6 Histogram Uji Evaluasi Waktu
Hancur Tablet
Pada Farmakope
Indonesia Edisi IV waktu hancur tablet yaitu tidak lebih dari 15 menit. Hasil
dari gambar menunjukkan bahwa semua formula memenuhi persyaratan waktu hancur.
Waktu hancur dari tiap formula berbeda-beda sebanding dengan kekerasan tablet.
Berdasarkan
hasil uji evaluasi tablet yang dilakukan yaitu uji evaluasi keseragaman bobot,
kekerasan, friabilitas, dan waktu hancur, tablet ekstrak jahe merah memiliki
kekerasan dibawah 4 kg, akan tetapi friabilitas, keseragaman bobot, dan waktu
hancur sesuai dengan persyaratan tablet. Faktor yang mempengaruhi kekerasan
tablet yaitu jenis dan jumlah bahan pengikat yang digunakan dan bahan aktif
yang digunakan. Akibatnya kompaktibilitas dan kompresibilitas massa tablet yang
akan dicetak rendah, sehingga kekerasan tablet berkurang (0,853 -2,49 kg).
Kekerasan tablet yang rendah tidak mengakibatkan friabilitas rendah, tetapi
baik (0,607 -0,85%). Waktu hancur bernilai 6.09 – 14.16 menit, masih memenuhi
rentang peryaratan waktu hancur tablet (<15 menit). Keseragaman bobot juga
memenuhi syarat, berarti homogenitas massa bagus. Secara umum dilihat dari
evaluasi, tablet ekstrak jahe merah memenuhi syarat farmasi industri dan
farmakope Indonesia Edisi III dan edisi IV.
BAB V
PENUTUP
A.
Kesimpulan
1.
Ekstrakjahemerah yang
dikombinasivitamin B6 dengan
berbagai jenis dan konsentrasi bahan pengikat dapatdibuatmenjadisediaan tablet
dengan metode granulasi basah.
2.
Hasil evaluasi tablet ekstrak jahe
merah menghasilkan kerapuhan, waktu hancur dan keseragaman bobot sesuai dengan
persyaratan evaluasi tablet tetapi kekerasan tidak sesuai dengan persyaratan
evaluasi tablet.
B.
Saran
Disarankan untuk peneliti selanjutnya dalam pembuatan tablet ekstrak
jahe merah dapat dilakukan uji stabilitas dan uji disolusi.
DAFTAR PUSTAKA
Allen L.V., Popovich N.G. and Ansel H.C.,
2014, Ansel, Bentuk Sediaan Farmasetis dan Sistem Penghantaran Obat,
Diterjemahkan oleh Lucia Hendriati dan Kuncoro Foe, Penerbit Buku Kedokteran
EGC, Jakarta.
Ansel H.C., 2014, Bentuk Sediaan Farmasetis
dan Sistem Penghantaran Obat, 9th (eds). Afifah, H.& Ningsih, T., Penerbit
Buku Kedokteran EGC.
BPOM RI, 2014, Persyaratan Mutu
Obat Tradisional, Peraturan Kepala Badan Pengawas Obat dan Makanan Republik
Indonesia, Indonesia, p. 1-25.
Ditjen BKAK. 2014. Farmakope Indonesia edisi V. Jakarta: Depkes RI.Hal.568.
Kumoro, A. C. 2015. Teknologi ekstraksi:
senyawa bahan aktif dari tanaman obat. Yogyakarta: Plantaxia. pp: 9-11.
Lette, I dan Jose, A. 2016. The Effectiveness Of Ginger in Prevention Of Nausea and Vomoting During Pregnancy and
Chemotherapy. Intergrative Medicine Insight. Libertas Academica. Hal. 15.
Parrott, L. (1971). Pharmaceutical Technology. United States
of America: Burges Publishing Company. Hal. 82.
Rahayu, Fitri. 2014. Formulasi Sediaan Chewabel Lozenges yang Mengandung Ekstrak Jahe Merah.
Fakultas Farmasi Universitas Muhammadiyah Surakarta: Surakarta
Saparinto, C dan Hesty, D.S. 201).
Jahe. Jakarta: Penebar Swadaya. Hal.
6-7
Saparinto, Cahyo & Susiana,
Rini. 2016. Grow Your Own Medical Plant – Panduan Praktis Menanam 51 Tanaman
Obat Populer di Pekarangan. Yogyakarta: Lily Publisher. Hal : 43-45.
Setyawan, Budi. 2015. Peluang Usaha Budidaya
Jahe. Pustaka Baru Press. Yogyakarta
Supriyanti, dkk. 201). Prinsip Obat Herbal.Edisi 1. Yogyakarta:
Cv Budi Utama. Hal. 1.
Zamroni Salim, Ph.D dan Ernawati
Munadi, Ph.D. 2017. Info Komoditi Tanaman Obat. Jakarta : Badan Pengkajian dan Pengembangan
Perdagangan Kementerian Perdagangan Republik Indonesia
- Dapatkan link
- X
- Aplikasi Lainnya












Komentar
Posting Komentar